过氧化氢制取氧气的化学方程式 实验室制取二氧化碳的化学方程式
本篇文章给大家谈谈过氧化氢制取氧气的化学方程式,以及实验室制取二氧化碳的化学方程式对应的知识点,希望对各位有所帮助,不要忘了收藏本站喔。
过氧化氢分解制取氧气的化学方程式 过氧化氢分解制取氧气的化学方程式怎么写
;?????
??????1、过氧化氢:化学式为H2O2。
??????2、二氧化锰催化过氧化氢分解,H2O2+MnO2+2H+=Mn2++2H2O+O2Mn2++H2O2=MnO2+2H+MnO2虽然参与了化应反应,但在反应前后质量和性质都没有发生变化,而且加快了反应速率,故二氧化锰是作为过氧化氢分解的催化剂。
??????3、过氧化氢分解制取氧气的化学方程式为:2H2O2(MnO2)=2H2O+O2↑。
过氧化氢制氧气的化学方程式
过氧化氢制氧气的化学方程式:
过氧化氢在金属氧化物的催化作用下,即可分解形成水和氧气。
过氧化氢制氧气化学方程式
过氧化氢制氧气的化学方程
式为:
2H2O2=MnO2=2H2O+O2(气体
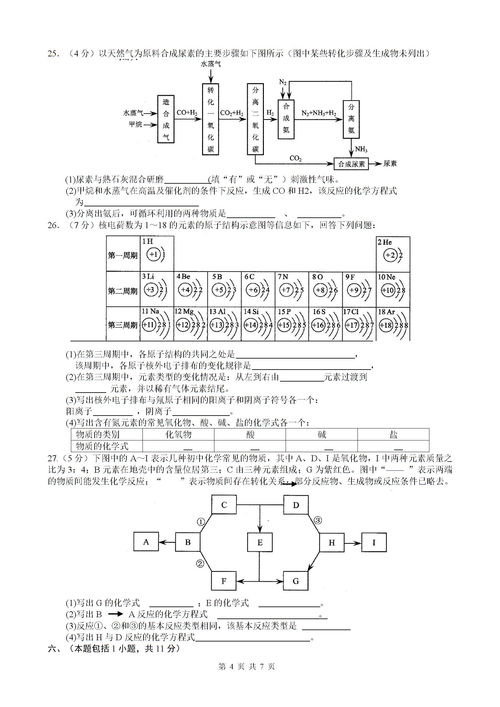
符号)
过氧化氢制取氧气的化学方程式
过氧化氢是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。过氧化氢制取氧气的化学方程式为2H 2 O 2 =2H 2 O+O 2 ↑。
过氧化氢制取氧气
实验药品:3%过氧化氢溶液、小木条、二氧化锰固体。
实验步骤
(1)在试管中加入少量过氧化氢溶液,把带火星的小木条放在试管口,观察现象(无明显现象)。
(2)在试管中加入少量二氧化锰,观察现象(出现大量气泡,木条复燃)。
(3)当停止生成气泡时,继续加入过氧化氢溶液,观察现象(出现大量气泡,木条复燃)。
(4)化学方程式:2H 2 O 2 =2H 2 O+O 2 ↑。
过氧化氢的性质
过氧化氢的化学式为H 2 O 2 。纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混溶,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。其水溶液适用于医用伤口消毒及环境消毒和食品消毒。过氧化氢溶于水、醇、乙醚,不溶于苯、石油醚。
纯过氧化氢很不稳定,加热到153°C便猛烈的分解为水和氧气。过氧化氢是一种极弱的酸:H 2 O 2 =(可逆)=H + +HO 2 - (Ka=2.4×10-12)。因此金属的过氧化物可以看做是它的盐。
h2o2制取氧气的化学方程式
过氧化氢制取氧气的化学方程式为2H 2 O 2 ==2H 2 O+O 2 ↑。过氧化氢是一种无机化合物,化学式为H2O2。纯过氧化氢是淡蓝色的黏稠液体,可任意比例与水混溶,是一种强氧化剂,水溶液俗称双氧水,为无色透明液体。
过氧化氢
其水溶液适用于医用伤口消毒及环境消毒和食品消毒。在一般情况下会缓慢分解成水和氧气,但分解速度极其慢,加快其反应速度的办法是加入催化剂——二氧化锰等或用短波射线照射。
在不同情况下有氧化作用和还原作用。用于照相除污剂;彩色正片蓝色减薄;软片超比例减薄等。极易分解,不易久存。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,过氧化氢在3类致癌物清单中。
过氧化氢制取氧气的化学方程式的介绍就聊到这里吧,感谢你花时间阅读本站内容,更多关于实验室制取二氧化碳的化学方程式、过氧化氢制取氧气的化学方程式的信息别忘了在本站进行查找喔。
本站文章为热心网友投稿,如果您觉得不错欢迎转载,转载请保留链接。网址:http://xzz5.com/z3093